近日,药学院吴云龙教授、吴彩胜教授团队与浙江大学平渊教授、中国人民解放军陆军军医大学徐祥教授合作,在可注射超分子水凝胶载体实现CAR-T细胞体内原位改造方面取得新进展,相关成果以“Injectable Supramolecular Hydrogels for In Situ Programming of Car-T Cells toward Solid Tumor Immunotherapy”为题在线发表在Advanced Materials杂志(DOI: 10.1002/adma.202310078)。

嵌合抗原受体T(CAR-T)细胞免疫疗法已成功应用于血液系统恶性肿瘤的治疗,然而其对于实体瘤的疗效仍远不能令人满意。其主要原因是由于传统的静脉输送方法使得CAR-T细胞优先被输送到靠近肿瘤的淋巴结和脾脏,而实体瘤由于其复杂的肿瘤微环境,静脉回输的CAR-T细胞难以有效富集到肿瘤附近,导致不能达到有效的杀伤效果。此外,CAR-T细胞体外改造再输回体内的方法,操作程序繁琐、周期长、成本高。
课题组设计了一种可注射、携带CAR质粒的超分子水凝胶体系(CD3-PPP/pCAR@α-CD),实现了CAR-T细胞的体内原位持续编辑和有效激活,并成功应用于人源化NSG小鼠模型中实体瘤的有效清除。相比于传统的静脉回输方法,这种CAR-T细胞体内原位局部编辑的方法操作简便,系统安全性强,在研究过程中未发现明显的细胞因子风暴。该策略不仅为实体瘤的细胞免疫治疗提供了一种新思路,还可应用于多种免疫细胞的局部基因改造。
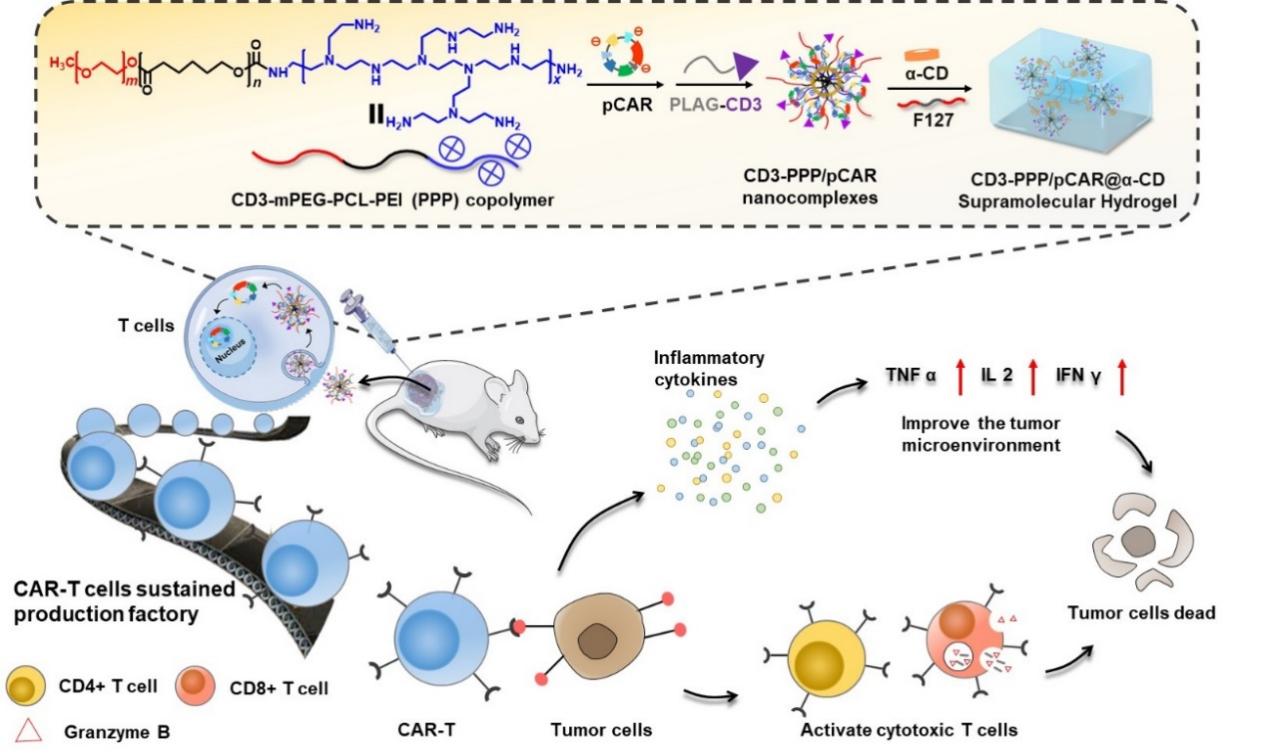
可注射超分子水凝胶剂型设计实现CAR-T细胞原位持续改造,促进实体瘤免疫治疗的示意图
目前,CAR-T细胞基因改造常用的方式为电穿孔或者病毒感染。电穿孔方式只能应用于体外,而用病毒载体进行体内改造又存在一定的安全隐患。课题组筛选发现mPEG-PCL-PEI(PPP)阳离子聚合物作为非病毒基因载体,能够有效地将CAR质粒递送入T细胞。在此基础上,课题组将含T细胞特异性启动子的叶酸受体(FRα)-CAR质粒与mPEG-PCL-PEI(PPP)阳离子长聚合物链共聚物通过静电相互作用络合形成纳米复合物,接着将T细胞靶向抗CD3ε F(ab’)2片段偶联到纳米复合物表面,最后利用α-CD与PPP之间的主客体相互作用,自组装形成超分子水凝胶。该超分子水凝胶载体经实体瘤瘤旁注射后,可持续释放携带pCAR的靶向纳米复合物(CD3-PPP/pCAR)原位编辑T细胞,如同一个“生产车间”,不断生产和积累CAR-T细胞。更为重要的是,相比于静脉输送CAR-T细胞在肿瘤部位累积少等难题,超分子水凝胶剂型对于CAR-T细胞在肿瘤部位的原位和持续改造,能够有效地促进肿瘤组织中CD8+和CD4+ T细胞的浸润,并通过增强促炎症因子(如IL-2、IFN-γ和TNF-α)和肿瘤杀伤蛋白颗粒酶B (GzmB)的表达来减弱实体瘤的免疫抑制微环境,增强抗肿瘤效果。
该研究证明了局部注射超分子水凝胶载体实现T细胞进行原位基因重编程的策略有利于实体瘤CAR-T细胞免疫治疗,为实体瘤的细胞治疗方法的开发提供了一定的参考。
该工作是团队近期关于自组装药物载体设计的最新进展之一。近年来,团队在超分子结构用于尺寸、性能可控载体设计的前期基础上(Angew. Chem. Int. Ed. 2009, 48: 3842; Acc. Chem. Res. 2013, 46: 782; Nanoscale 2016, 8: 18876),设计多嵌段聚合物及其自组装形成的纳米胶束结构,高效地利用静电和疏水相互作用包裹并稳定治疗基因质粒(Small Methods 2021, 5: 2100347);在提升基因转染效率的同时诱导靶蛋白的表达,进而显著减弱肿瘤耐药性(Chem. Eng. J. 2023, 453: 139879)。团队还进一步探索高分子药物递送载体设计及其在剂型改良药物方面的应用(ACS Nano 2023, 17: 9826; Mil. Med. Res. 2023, 10: 37),设计合成有良好生物相容性的两亲性聚氨酯自组装纳米胶束、自组装超分子水凝胶、多臂环糊精衍生化单分子胶束,实现难溶药物、活性大分子的稳定包封以及药物生物利用度提升(Adv. Mater. 2022, 34: 2107674; Bioact. Mater. 2022, 9: 77; Adv. Healthcare Mater. 2023, doi: 10.1002/adhm.202302153)。
全文链接:https://doi.org/10.1002/adma.202310078

