细胞应激生物学国家重点实验室、福建省药物新靶点研究重点实验室、药学院高祥副教授团队与合作者在高灵敏度蛋白质定性和定量分析技术方面取得重要进展,相关成果以“Isobaric Stable Isotope N-Phosphorylation Labeling (iSIPL) for Ultrasensitive Proteome Quantification”为题在线发表在Angew Chemie International Edition杂志(DOI:10.1002/anie.202303656)。

基于质谱技术的蛋白质组学在蛋白质结构与功能研究、生命化学本质的揭示、人类重大疾病的诊断及新药研发等方面提供了重要技术支撑。虽然多种蛋白质定量分析方法相继建立,但蛋白质的精准定量和深度覆盖仍然是当今蛋白质组学研究面临的挑战,特别是在微量蛋白定量分析方面,如单细胞水平蛋白质组学分析、蛋白-蛋白相互作用、蛋白翻译后修饰及临床微量样本分析等,发展高灵敏度蛋白质定性和定量分析组学质谱技术具有重要科学意义。高祥团队通过近十年的联合攻关,研发出一种等重稳定同位素标记磷试剂(iSIPL)蛋白质定量技术,其化学结构源于赵玉芬院士提出的核酸与蛋白共起源N-磷酰化氨基酸化学模型,利用了中性磷酰基团高质子亲和能特性,在较低裂解能量下产生具有P-N化学键独特结构的磷酰胺报告离子对(m/z 180/181和m/z 208/209),具有双重定量功能,为蛋白质的高灵敏精准定量提供了磷化学新策略。
iSIPL磷试剂具有极好的稳定性、重复性和蛋白标记效率,在肽段测序、微量蛋白鉴定和定量方面具有显著优势。在微量标准蛋白分析中,iSIPL磷试剂能够鉴定到更多的肽段种类和获得更高的蛋白覆盖率;在对微量复杂细胞总蛋白的分析中同样能够鉴定更多的蛋白质种类。另外,其报告离子对可以提供双重定量信息,提升了蛋白定量结果的可靠性与准确性。同时,研究团队应用两标iSIPL磷试剂,对HIV-1潜伏病毒基因转录激活前后蛋白激酶CDK9相互作用蛋白库进行了定量分析,成功发现并验证了CDK9互作新蛋白PARP13在HIV-1潜伏基因转录延伸激活过程中发挥的调控作用。
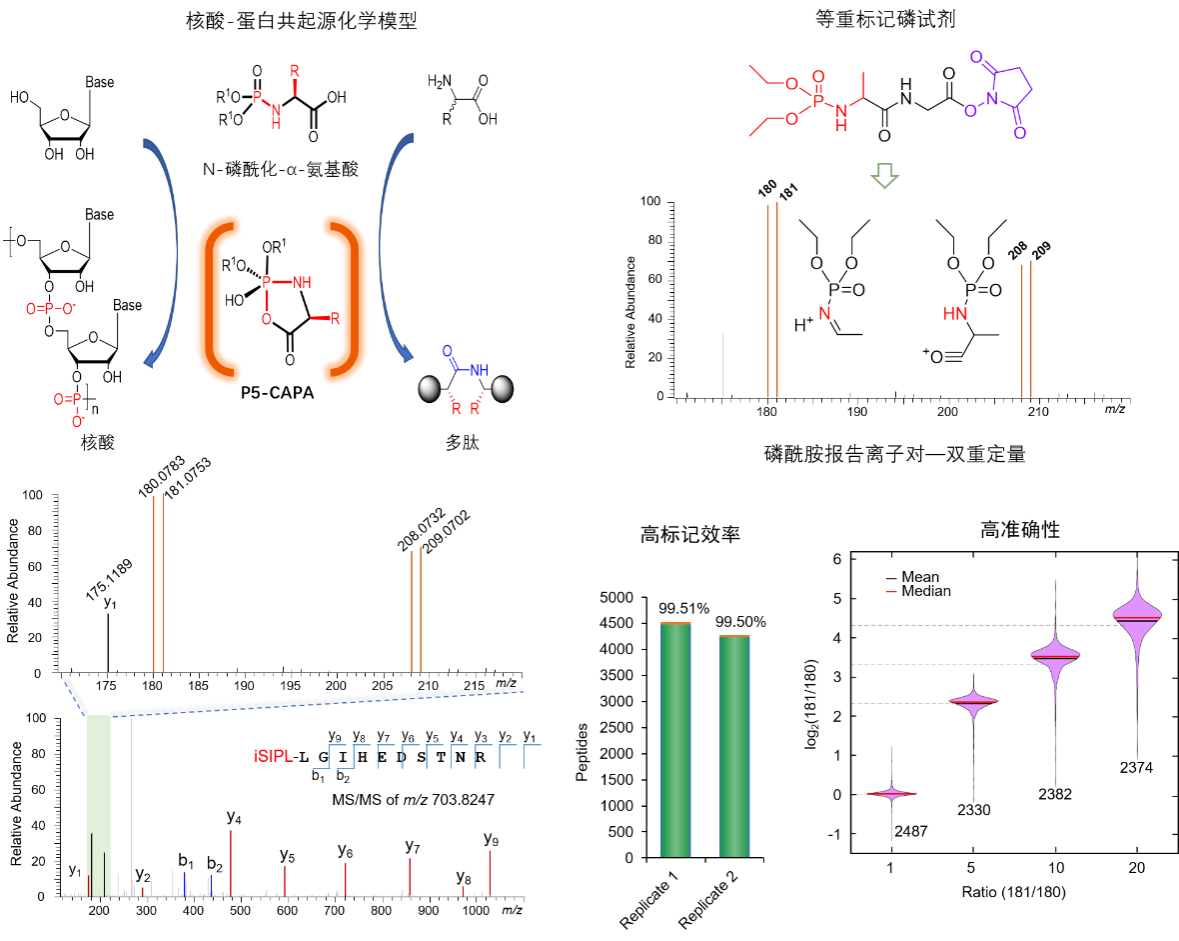
基于iSIPL磷试剂结构可以实现不同位置稳定同位素的高效引入,为开发多标定量磷试剂提供了优越的结构基础,且极大降低了商品化等重标记试剂高昂的价格成本。本论文相关研究成果已获授权国家发明专利三项,国际PCT专利一项,均已实现技术转化,并基于原创磷试剂技术成功研发系列磷试剂产品,打破国外相关同类型试剂近二十年的市场垄断。iSIPL等重标记磷试剂基于N-磷酰化氨基酸的原创磷化学理论体系,实现微量蛋白组样品的高灵敏定性和精确定量质谱分析,在生命定量分析、新药物研发及临床疾病诊断等研究领域中具有广阔的应用前景。

厦门大学药学院高祥副教授、加州大学伯克利分校周强教授(现工作单位为香港大学理学院)和厦门大学电子科学与技术学院董继扬教授为本文共同通讯作者。厦门大学药学院为第一通讯单位,厦门大学博士研究生王晓宇(药学院与化学化工学院联合培养)、药学院博士后陈春景、何耀辉为共同第一作者。该研究得到了化学化工学院赵玉芬院士及药学院刘文教授的大力支持。该研究得到国家重点研发计划项目(2020YFA0608300)、国家自然科学基金(22274136, 92256203, 21305115, 81871445, 91856126)、厦门南方海洋研究中心(17GYY002NF02)、中国科学院空间利用技术与工程中心(No. YYWT-0901-EXP-16)及厦门大学校长基金(20720170069)等多个项目的经费支持。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202303656
(图/文 高祥课题组/江杉)

