厦门大学曾骥孟团队在国际知名期刊LEUKEMIA发表“一种新型CAR-T-CDR3个体化免疫治疗急性T淋巴细胞白血病(ALL)”的研究成果
4月8日,Nature Journals自然旗下血液学期刊LEUKEMIA(JCR1区、IF 12.104)在线刊出了厦门大学药学院曾骥孟教授团队发表的题为“Unique CDR3 epitope targeting by CAR-T cells is a viable approach for treating T cell malignancies”的研究论文。该研究利用免疫组学和高通量测序技术,对急性淋巴癌肿瘤(T-ALL)特异性TCR CDR3新抗原(Neoantigen)克隆进行表位筛查,设计出了靶点CDR3的CAR-T,为治疗T淋巴细胞系列的恶性肿瘤提供了免疫T细胞结合新抗原的临床实践新思路。
文章是在曾骥孟教授领导的转化医学中心团队(TMRC)与美国Scripps研究所Dr. Lerner病毒免疫实验室合作框架下,攻克T细胞型急性淋巴癌的免疫治疗所需肿瘤靶标新抗原的寻找与临床转化,该论文是双方实验室在免疫细胞诊疗与临床转化的长期合作成果之一。
白血病是造血干细胞水平的克隆性恶性疾病,造血干细胞移植、化疗等医疗手段为血液肿瘤的治疗带来革命性的进步。然而,相对于治疗慢性髓细胞白血病以格列卫(Gleevec)靶向药物为代表的抑制剂以及单克隆抗体药物等在B淋巴细胞白血病(B-ALL)的临床应用,人类在攻克生物侵袭性更强的急性T淋巴细胞白血病(T-ALL)上收效甚微,为提升该病的整体疗效和预后,需要进一步拓展思路。目前政府出台的有关免疫细胞治疗的新政策也为这项成果的临床试验开辟了绿色通道, 以拯救更多血液肿癌患者。
T系肿瘤是一类涵盖急性T淋巴细胞白血病、成人T细胞白血病/淋巴瘤、外周T细胞淋巴瘤等、蕈样莓菌病等22个临床亚型的恶性血液系统肿瘤,占所有淋巴系统恶性肿瘤的15-25%。在人类T淋巴细胞白血病淋巴瘤病毒(HTLV-1)流行的福建/台湾沿海地区等地,该恶性血液病防控局势极为严峻。相比B细胞系肿瘤,其对于传统的化疗与靶向药物的不敏感,移植机会缺乏,个体间病程差异很大,促使人们去研究免疫性靶向治疗在该病中的可能用途。
曾骥孟教授团队一直在寻找T-ALL潜在的治疗靶点新抗原-----一种能够区分白血病T细胞与正常T细胞的特定蛋白,这意味着该疗法通过靶向这个特定蛋白,仅攻击白血病T细胞(癌症细胞),而对正常的免疫系统T细胞不造成严重损害。
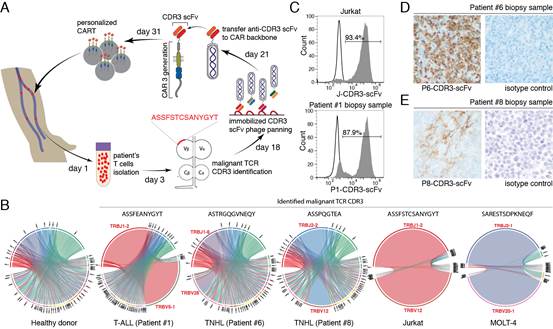
曾骥孟教授课题组,首先采用高通量测序技术对T系肿瘤患者TCR β链的抗原互补决定区(CDR3)进行免疫组学测序,发现T系肿瘤患者体内存在个体特异性肿瘤克隆,即一个具有相同CDR3的恶性细胞群体。利用独特型-抗独特型免疫网络调控的原理,构建了T系肿瘤噬菌体展示ScFv抗体库,并成功筛选出靶向CDR3的抗体序列。利用该抗体序列,采用嵌合抗原受体T细胞技术(CAR-T)体外基因编辑重组T细胞表达Anti-CDR3-CAR-T,证明它在体外试验和疾病动物模型中是有效的,实现了对T系肿瘤细胞株和白血病原代细胞的特异性杀伤,明显降低疾病模型体内的肿瘤负荷(TMB),显著延长生存期。
过去,曾骥孟教授课题组曾运用Anti-EGFR-Car-T及Car-T-NK/MSN技术于实体肿瘤(脑胶质瘤GBM与肝癌HCC)治疗, 这次课题组的成果是国际上首次尝试CDR3 epitope作为血液瘤靶标潜能。该课题亦获得了国外科研机构的支持,其中包括美国SCRIPPS研究院及俄罗斯科学院等。目前, 该团队正在积极推进CDR3临床精准医学转化,并已完成WHO中国临床实验注册中心的申报工作及进行CRO/cFDA 临床试验咨询委员会会议。

