2025年9月9日,厦门大学药学院李明玉教授团队受邀在Cell Press旗下内分泌代谢领域期刊Trends in Endocrinology &Metabolism杂志上发表题为“Glucagon receptor antagonism requires further mechanistic attention on α-cell physiology”的论坛综述,论文系统总结了李明玉教授团队及国际同行近年在由胰高血糖素受体(GCGR)信号通路介导的肝脏-胰岛α细胞轴的研究进展,梳理了GCGR拮抗剂与α细胞代谢之间的关系,以及GCGR拮抗剂在糖尿病治疗领域的研究现状与面临的挑战,并在此基础上展望了未来的研究方向。
胰高血糖素是一种主要由胰岛α细胞分泌的肽类激素,在血糖稳态中充当胰岛素的功能拮抗者。它通过与肝细胞表面的GCGR结合,激活细胞内信号通路,促进肝糖原分解和糖异生,从而提高血糖水平。胰高血糖素-GCGR信号异常已被证明是糖尿病发生发展的关键因素之一。多项动物实验和临床试验结果显示,GCGR拮抗均能显著改善1型和2型糖尿病模型的血糖水平,同时降低餐后血糖波动并改善糖化血红蛋白水平。
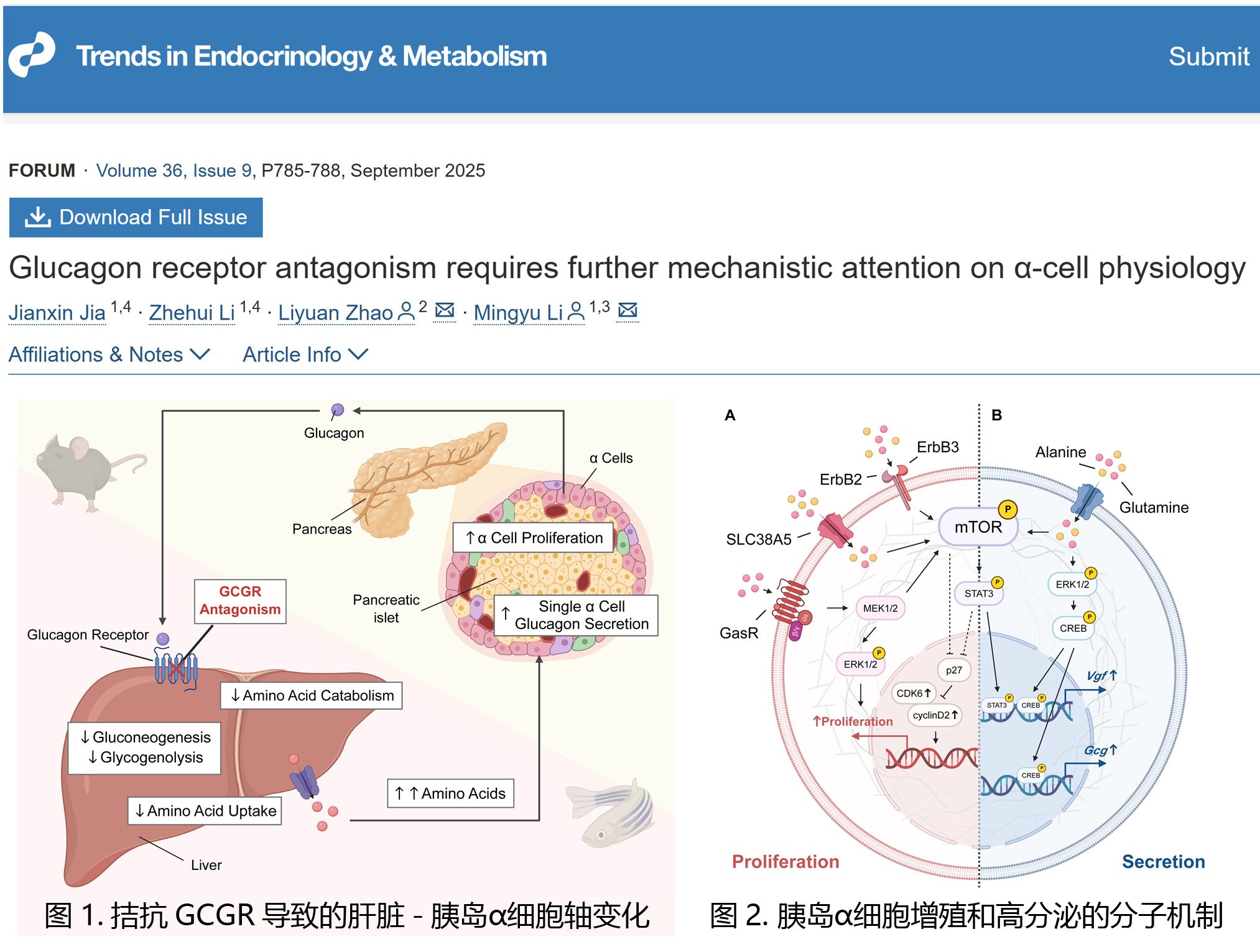
然而,GCGR拮抗剂尚未获批用于临床治疗,其关键限制因素在于可能引发α细胞增生、高胰高血糖素血症、氨基酸代谢异常及脂质代谢紊乱等多重不良反应。这些不良反应的发生与肝脏-α细胞反馈轴的失衡密切相关。GCGR拮抗剂会破坏这一反馈环路,导致肝脏氨基酸摄取和代谢能力下降,血清氨基酸水平升高,进而通过多种信号通路刺激α细胞增生。研究表明,α细胞增加SLC38A5的表达,通过L-谷氨酰胺依赖的mTOR通路诱导细胞增殖是增生的重要机制之一。2024年8月李明玉教授团队在Journal of Biological Chemistry杂志发表的研究进一步揭示,ErbB3/ErbB2复合物可通过激活mTOR和STAT3等下游效应器,促进cyclin D2表达、抑制p27水平从而推动α细胞增殖。
研究团队发现GCGR拮抗剂不仅诱发α细胞增殖,还导致α细胞单细胞水平的胰高血糖素过度表达与分泌。通过GCGR敲除斑马鱼和GCGR敲除小鼠胰岛的单细胞转录组测序,团队研究证实GCGR拮抗后胰岛α细胞的胰高血糖素表达水平大量上升,从而导致分泌异常增加。分子机制研究发现,Vgf基因在α细胞中特异性高表达,其功能抑制可显著降低α细胞的胰高血糖素过度分泌。进一步实验显示,氨基酸驱动的mTOR-STAT3与ERK1/2-CREB信号共同作用于Vgf和Gcg基因表达,促进胰高血糖素颗粒生成和分泌,从而通过α细胞增殖与单细胞过度分泌共同驱动高胰高血糖素血症产生,相关研究成果先后发表于Journal of Biological Chemistry(2022年12月)和Nature Communications(2025年3月)。

这些研究不仅深化了对GCGR及肝脏-α细胞反馈轴的认识,也为糖尿病治疗策略优化提供了新的科学依据。未来,通过进一步探索GCGR调控及下游信号通路的精细化干预,聚焦GCGR选择性拮抗剂/激动剂的药物开发研究,将为临床开发更安全、高效的糖尿病治疗方案奠定重要理论基础。
相关论文链接:
https://www.sciencedirect.com/science/article/abs/pii/S1043276025001547;
https://www.nature.com/articles/s41467-025-57786-7;
https://www.jbc.org/article/S0021-9258(24)02000-3/fulltext;
https://www.jbc.org/article/S0021-9258(22)01108-5/fulltext
